О самодельном свинцово кислотном аккумуляторе
Первый свинцово кислотный аккумулятор изобрел и опробовал как известно французский физик Гастон Планте. Он скрутил две свинцовые пластины в рулон, предварительно проложив между ними разделительное сукно. Рулон поместил в сосуд и залил его соленой водой. В итоге если подать напряжение на пластины, то он заряжался. И после, если к нему подключить лампочку, или что-то другое, то он мог некоторое время отдавать запасенную энергию на горение этой лампочки. Так же после заряда энергия в таком аккумуляторе могла хранится без потерь продолжительное время. Это и положило начало эры свинцово кислотных аккумуляторов.
Но самый главный недостаток такого рулонного аккумулятора, это маленькая емкость. В последствии было выяснено что если такой аккумулятор несколько раз зарядить и разрядить меняя полярность (+-), то емкость увеличивалась. Это объясняется тем, что на пластинах образовывался слой оксида свинца, и пластины размегчаоись, становились как губка. Кислота теперь могла проникать глубже в пластины, тем самым больше свинца участвовало в химическом процессе.
Эти циклы заряда разряда меняя плюс на минус и обратно назвали формовкой пластин. Чтобы нарастить толстый слой оксида свинца, приходилось затрачивать много энергии и времени. Но позже один молодой человек, работавший помощником у Планте решил сделать по другому. Он решил сразу наносить на пластины оксид свинца, тем самым он сразу получил более емкий аккумулятор. В последствии эту технологию немного улучшили. Стали делать свинцовые решетки, которые замазывали аксидом свинца в виде пасты. Пасту готовили из оксида свинца, в которую добавляли немного воды, или электролита и перемешивали до густой консистенции.
Спустя уже более 100 лет технология изготовления аккумуляторов в принципе не изменилась. На производствах так же методом литья, или штамповки делают свинцовые решетки, и намазывают пастой, состоящей из оксида свинца, плюс дополнительные добавки, которые не дают пасте распадаться и придают другие нужные свойства. Так же разделительные прокладки между пластинами делают из современных материалов, что исключает выпадение намазки из решеток и препятствует замыканию пластин между собой. На каждом заводе, и для различных типов аккумуляторов ( тяговых, стартерных, и т.п.) есть свои тонкости, но в целом технология одна и та же.
Теперь можно подумать о том, можно ли сделать свинцово кислотный аккумулятор в домашних условиях, чтобы это было выгодно и эффективно. Во первых дело в свинце, где его брать?. В негодных аккумуляторах, но если переплавить один авто-аккумулятор, то на выходе будет всего примерно 1,5кг свинца, и станет понятно что добывать свинец таким образом не выгодно. Чтобы переплавить весь свинец содержащийся в аккумуляторе, часть которого в виде оксида, сульфата и прочие элементы, которые содержатся в намазке решеток, то тут нужна плавильная печь и дополнительная химия и условия, по-этому дома на костре получится консервная банка свинца и целая куча шлака.
Тогда можно купить свинец, есть листовой, и в чушках, стоит не дорого. Если делать из листового свинца, то можно примерно прикинуть затраты на один аккумулятор. Если покопаться в литературе, то можно узнать что с одного квадратного метра площади пластин можно получить емкость примерно 5-10Ач. Тогда для одной банки емкостью 50-100Ач нужно 10кв.м свинца. Так как для 12-ти вольт нужно 6 банок, то соответственно нужно около 60 кв.м свинца. Самые тонкие листы в продаже 0,5мм, вес одного кв.м такого листа свинца состовляет 5,7 кг. Так как площадь листа работает с обоих сторон, значит нам нужно на АКБ уже не 60кв.м, а 30кв.м. Тогда получается на аккумулятор емкостью 50-100Ач нужно 30*5,7=171кг свинца, стоимость за 1кг около 150 рублей, и цена только на свинец составит около 25 000 рублей, что в 5-6раз дороже чем заводской аккумулятор емкостью 100Ач.
Можно увеличить емкость пластин формовкой, с помощью зарядки и разрядки меняя местами плюс и минус, но не известно сколько циклов нужно сделать чтобы значительно увеличить емкость. Планте формовал пластины электричеством три месяца. За это время уйдет очень много энергии на формовку, и в итоге аккумулятор только подорожает. Из всего этого понятно что экономически не выгодно делать аккумулятор из листового свинца.
Да, кстати на счет долговечности аккумулятора с пластинами из листового свинца. Служить такой аккумулятор будет значительно дольше, так-как пластины цельные и от глубоких разрядов, больших разрядных токов, не будет отходить намазка, которой просто нет, но сульфатация пластин будет точно такая же как и у обычного аккумулятора, по этому по сути дольше обычных этот аккумулятор не прослужит. Правда его можно разобрать и почистить от белого налета (сульфата) и он дальше сможет работать.
Проблема в том что у листового свинца нет слоя оксида, точнее есть, из-за него свинец становится темно серого цвета, но этот слой слишком тонкий. Оксид, это окисленный кислородом свинец, на производствах его по разному получают. Но в домашних условиях эту пыль получить затруднительно. Можно конечно попробовать пластины увлажнять водой, чтобы они окислялись на свежем воздухе, но какой слой окиси удастся нарастить таким образом и сколько времени на это уйдет не известно, поэтому про рулонный аккумулятор из листового свинца можно забыть.
Хороший аккумулятор получится если использовать вместо пластин свинцовую фольгу. Так можно в несколько раз увеличить площадь при том же весе, но дома фольгу не сделаешь, а в продаже чистой свинцовой фольги нет, да и стоила бы она в несколько раз дороже листового свинца того же веса. Поэтому хороший вариант с фольгой отпадает. Или дома ставить прокаточный станок и самому делать фольгу.
Можно попробовать делать пластины как делают на заводе, решетки отлить не сложно. Они толстые, и форму для отливки сделать просто. Но проблема в намазке, она ведь состоит из оксида свинца, а как его делать дома. К примеру чем нибудь стирать свинец в пыль, или мелкую стружку, потом поливать водой или электролитом и в какой нибудь емкости его постоянно перемешивать чтобы окислялся на кислороде, но это дома трудно и бессмысленно делать, так как готовый аккумулятор гораздо дешевле выйдет.
Вот наверно вкратце все что я хотел сказать. Для себя я сделал вывод что свинцовый аккумулятор своими руками возможен, но трудоемок и не выгоден, поэтому на этом деле можно смело ставить большую и жирную точку. Так же читая множество информации и о других типах аккумуляторов я пришел к выводу что ничего нормального в домашних условиях и с применением доступных и дешевых материалов не выйдет. Если есть вопросы или какие-то выводы то оставляйте комментарии.
Источник
Как сделать аккумулятор своими руками
Есть множество способов сделать самодельные батарейки. К сожалению, большинство самодельных аккумуляторов либо бесполезны, либо потенциально опасны и сложны в изготовлении. Батареи из лимона и картофеля, как правило, очень слабые и требуют в качестве материала скоропортящегося органического растительного материала, в конструкцию свинцово-кислотных аккумуляторов входят высокотоксичные и едкие химикаты и т.д.
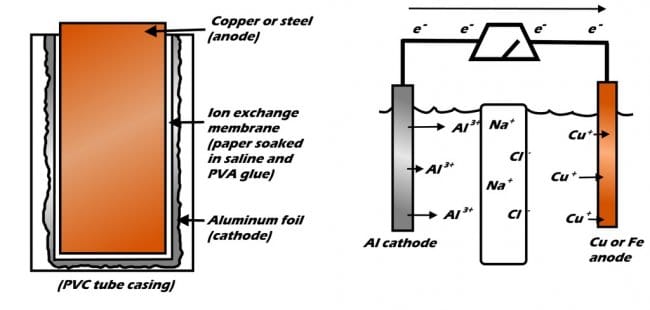
Эта батарея сделана из очень простых и доступных материалов, и обладает достаточной мощностью для работы устройств. Когда традиционные батареи недоступны эта батарея будет отличным аварийным источником электроэнергии. Кроме того, ее можно легко перезарядить практически от любого источника постоянного тока, она очень легкая и, в отличие от более распространенных алюминиево-воздушных батарей, не требует воздушного потока для работы.
Шаг первый: дизайн и теория
Принцип работы батарей основан на химической реакции, известной как окислительно-восстановительная реакция. В окислительно-восстановительной реакции одно вещество окисляется (теряет электрон), а другое восстанавливается (приобретает электрон). Довольно просто. Любая батарейка устроена схожим образом, в ней обязательны три элемента, между которыми происходит химическая реакция, в результате которой возникает электричество: электроды — анод, катод, и электролит.
В этой алюминиево-металлической батарее две половины батареи пропитаны физиологическим раствором и разделены специальной мембраной, пропускающей только ионы натрия и хлора. Алюминий с одной стороны начинает окисляться, в то же время как медь или сталь на противоположной стороне пытаются остаться стабильными.
В принципе любая батарейка или аккумулятор это две металлические пластины, помещенные в специальное химическое вещество – электролит. Одна пластина подключается к плюсу, вторая к минусу. Пока батарею не трогают, на ней остается стабильное напряжение, например, 3 или 9 В. Стоит подключить к батарейке нагрузку, лампочку, вентилятор, как от плюса к минусу потечет ток. Напряжение начнет падать и сразу же начнется окислительно-восстановительная реакция. Электроны начнут перетекать с отрицательной (-) пластины обратно на положительную, поддерживая тем самым разность потенциалов между ними.
Реакции бывают обратимыми (аккумулятор) и необратимыми (батарейка). Т.е. в батарейке реакция необратимая и ее нельзя зарядить, а в аккумуляторе обратимая и он заряжается. Если подключить аккумулятор к зарядному устройству, ток внутри него начинает течь в обратном направлении, то есть – от «+» к «-». И реакция в электролите также начинает идти в обратном направлении. В результате, продукт реакции разлагается на исходные вещества. Аккумулятор «заряжается»
Конечно, этот процесс не бесконечен и наступит момент, когда одна из пластин разрушится и химическая реакция больше не сможет проходить.

Шаг пятый: зарядка и проверка
Аккумуляторная батарея готова, но ее нужно зарядить. Можно использовать практически любой источник постоянного тока, если ток не слишком велик (до 5 А). Чтобы зарядить аккумулятор, нужно подключите анод к плюсу зарядного устройства, а катод к минусу. Во время зарядки ток начнет уменьшатся по мере того, как батарея набирает заряд. Это является хорошим признаком, и говорит о том, что батарея работает правильно. После зарядки нужно проверить аккумулятор мультиметром. Используя медный анод, мастер получил максимальное напряжение 1,44 В после скромного цикла зарядки. Максимальный ток, который он получил от батареи, был большим для такой самодельной батареи — 1.2 А. Для сравнения, лимонные или картофельные батареи обычно выдают в лучшем случае всего несколько миллиампер. Коммерческая батарея D-cell может выдавать ток более 5А.
Так же мастер провел тест, в котором сравнил свою батарею с настоящим D-элементом на 1,5 В. Обе батареи тестировались с небольшим двигателем постоянного тока. При этом измерялся ток и скорость вращения двигателя. И самодельная и промышленная батареи показали примерно одинаковые результаты.
Конечно, этот аккумулятор не идеален. Ионообменная мембрана по-прежнему пропускает некоторые растворимые соли меди на катодную сторону батареи, где они вступают в реакцию с образованием металлической меди и нерастворимых оксидов и гидроксидов меди. Кроме того, алюминиевый катод постепенно приходит в негодность, по сути, растворяется. Но, несмотря на это, батарея очень удобна и может быть легко собрана и использована людьми в экстремальной ситуации. Увеличивая размер батареи, и подключая несколько ячеек последовательно или параллельно, можно производить или хранить очень большое количество энергии с небольшими затратами.
Источник
Самодельный свинцово-кислотный аккумулятор
Мужик переплавил пластины и сам собрал свинцовый аккумулятор:
https://electrotransport.ru/ussr/index.php?topic=52527.216
«гоняю их в зад перёд. 2 в паралели, 100 и 200 А. розряжаю компом или теликом бывает лампочками. Умудрился от АКБ этих закипятить чашку чая гдето 450 гр. температура воды была нуливая. кипятильник 500 ватт. напруга просела до полного кипения 10.8 в. зато радости было полные штаны»
«Ёмкость растёт потихоньку. По ходу ещё долго будет рости, наверно до следующей осени.»
«радует то что не здря промучался целое лето»
«Собери весь этот хлам, переплавь как я. Сделай нормальную форму для отливки решоток и будет тебе счастье. А про магазинские ЗАБУДЬ. Они негодные«
—-
Многие спорят: существует единое мировое правительство или нет?
По таким косвенным признакам понятно, что оно существует. Хотя контролирует не всё подряд, но некоторые направления развития контролирует очень жёстко (на уровне «если пойдёшь туда, мы тебя убьём»).
В частности, полностью запрещена разработка ёмких и одновременно дешёвых аккумуляторов. И даже проверенные технологии столетней давности намеренно ухудшаются:
http://xaliavschik.livejournal.com/775028.html
И ценообразование на этом рынке искусственное. Как может банка панцирного свинцового аккумулятора стоить дороже жёсткого компьютерного диска? Этот диск — сложнейшее изделие точной механики, а в аккумуляторе ничего сложного нет, вон кулибины легко собирают его на коленке.
Источник
Самодельный аккумулятор
Спанч-боб
В любом случае — полезно уметь делать аккумуляторы своими руками.
(поташный, газовый аккумулятор. )
Причём в стационарных условиях их можно сделать огромных размеров.
Предлагаю обсудить тему:
Как изготовить самодельный аккумулятор электрической энергии?
Вопросы
— Какие виды аккумуляторов возможно сделать самому на «коленке»?
— Какие материалы/кислоты/щелочи стоит запасти?
— Какая есть литература по этому вопросу?
— Есть ли аккумуляторы которые можно хранить без ущерба для ресурса? Например сухозаряженный
Да. Изучить устройство древней «багдадской батареи».
http://ru.wikipedia.org/wiki/%. %F2%E0%F0%E5%FF
Причем електролит может очень варьироватся, как и конструкция стержней — я в радиокружке в детстве подпаивался к железному и латунному ключам и прочему мотлоху засунутому в стакан и.
Lev007
— Какая есть литература по этому вопросу?

«Батареи и аккумуляторы для радиоприёмников» [Спижевский И. 1937] http://publ.lib.ru/ARCHIVES/S/. vskiy_I.I..html
В последнее время, чтобы аналог чего-то массово выпускающегося собрать, обычно нужно купить материалов на сумму несколько большую чем стоит готовое изделие. При этом знания и инструмент для обработки и сборки в цену считаем что не входят. «Цена в партии от 1000 штук» и т.п. имеют значение. Поэтому я бы отделил вопрос «знать и уметь» от непосредственно «Какие материалы/кислоты/щелочи стоит запасти».
jim hokins
Проще и ДЕШЕВЛЕ запасти уже ГОТОВЫЕ аккумуляторы.Сухозаряженные свинцово-кислотные,щелочные или никельбметаллгидрид Санйо Энелуп(хранятся в заряженном состоянии до 5 лет).
Это понятно, я о том же писал, но знать из какого говна и каких палок можно слепить что-то годное — тоже дорогого может стоить. Опять же, где как не в палате найдешь ссылку на книжку 37-го года?
Проще и ДЕШЕВЛЕ запасти уже ГОТОВЫЕ аккумуляторы.Сухозаряженные свинцово-кислотные,щелочные или никельбметаллгидрид Санйо Энелуп(хранятся в заряженном состоянии до 5 лет).
Санйо Энелуп запасено.
Вот сколько лет могут хранится сухозаряженные свинцово-кислотные аккумуляторы?
А по теме, скажем так, для общего развития, чтобы знать и уметь 😊
Кстати где-то видел информацию по кустарному изготовлению гелевых аккумуляторов из обычных свинцовых.
Lev007
Кстати где-то видел информацию по кустарному изготовлению гелевых аккумуляторов из обычных свинцовых.
Lev007
сколько лет могут хранится сухозаряженные свинцово-кислотные аккумуляторы?
Lev007
кустарному изготовлению гелевых аккумуляторов из обычных свинцовых.
jim hokins
Современый ширпотреб,-не в курсе.Бывают прям из магаза никудышние,о каком хранении может идти речь?
Гелезируются свинцокислые заливкой обычного водного кремнекислого натрия — строительного жидкого стекла чтобы подешевле и большими банками продавалось. Конечно это череповато внесением грязи и сокращением ресурса еще больше, а доставать химически чистую гелезирующую химию имхо мало кто будет.
Смысл гелезации заливных — использование в разных пространственных положениях чтобы обходиться без проливания электролита. Иногда это важно.
Сухие приличные могут храниться как минимум единицы лет — но надо закрывать герметично и исходно сильно высушить. Намного дольше и лучше хранятся никелевые — и новые и бу. Обычно их малоимущие в текущей северной папуасии на месте бывшего совка успешно пользуют даже после десятков лет валяния на помойках, а перед этим их еще регулярно могли промывать жижей из грязных канав и заливать техническими грязными электролитами. Проржавевшие до дыр стальные корпуса восстанавливаются например обтягиванием нагретой пластиковой бутылкой сообразного размера или заливкой расплавом битума в облегающую корпус ржавой банки пластиковую бутылку.
Книжки из начала совка были важны и пригодны в фазе разгорания вспышки техноцивилизации.
А сейчас фаза завершения — тута имеются в доступности наработанные недавно прошедшей техноцивилизацией большое количество артефактов — и по электрохимическим устройствам. Теперь имхо важнее учиться как из отходов собирать действующие акб например. Из выброшеных на помойку свинцокислых еще удается выплавить много свинца для изготовления поверхностных пластин. Где-то должны быть большие запасы хотя бы технической серной кислоты чтобы сделать электролит.
Для никелевых акб важны умения ремонтировать ламельные конструкции для устранения коротких замыканий и перекорпусения из прогнивших стальных банок из просравшей полимеры империи зла в доступные пластиковые емкости поступающие на свалки после выключения железного занавеса. Да хоть в деревянные кадки пропарафиненые с пригнанными плотно крышками.
Смысл примерно как и про патроны — в 18хх годах патронов еще было меньше населения, а щас их уже по слухам больше и после чистящего писца возможно запасов уже изготовленых акб останется также больше чем населения которым они еще нужны.
Теперь имхо важнее учиться как из отходов собирать действующие акб например. Из выброшеных на помойку свинцокислых еще удается выплавить много свинца для изготовления поверхностных пластин.
Вот! Вот об этом стоит поговорить поподробнее.
Теперь имхо важнее учиться как из отходов собирать действующие акб
вопрос: зачем ТС хочет изготавливать АКБ?
текущие умрут лет через 5-10, да и не умрут. а потеряют емкость в большистве. С учетом того, что мощные потребители эл-ва умрут еще раньше, то остатка хватит надолго.
Тут уж либо технология восстановится и запустят завод АКБ, либо они не будут нужны.
Ну при попытке использования автомобильных свинцокислых в автономной системе им уже может сильно поплохеть через 2..3 цикла и пару недель при нарушении режима заряда. Так что 5 лет это экстремально оптимистичное время для случая использования стартерных свинцокислых с намазными пластинами.
А у вариантов с поверхностными пластинами удельная емкость по массе и обьему в десятки раз хуже текущих автоакб стартерных. Так что даже для батарейки скромной емкости надо будет свинцу собирать и транспортировать много.
Поиск листового цинка, как мне кажется, задача непростая.
Цинк можно электролизить из солей. И будет тоже аккумуляция элэнергии.
Во время ВОВ восстановление стартерных АКБ (по факту — изготовление новых) производилось в войсках, вероятно на уровне ОРВБ дивизии — АРЗ армии (фронта).
Отливались новые решетки, активная масса (ЕМНИП Pb + PbO) размалывалась в мельницах и наносилась на решетки. Формовались пластины. Понятно, что срок службы таких АКБ был мизерным, но, вероятно, был организован сбор неисправных.
А из необычных химических источников тока недавно видел следующий: к выводам светодиода подпаяны проволочки из разноименных металлов и воткнуты в какой-то фрукт. Кислый сок — в достаточной степени электролит. Вот не знаю, правда или нет.
Nikola_spb
из необычных химических источников тока недавно видел следующий: к выводам светодиода подпаяны проволочки из разноименных металлов и воткнуты в какой-то фрукт. Кислый сок — в достаточной степени электролит. Вот не знаю, правда или нет.
Lev007
— Какие виды аккумуляторов возможно сделать самому на «коленке»?
— Какие материалы/кислоты/щелочи стоит запасти?
— Какая есть литература по этому вопросу?
Radmir
где как не в палате найдешь ссылку на книжку 37-го года?
Все более чем реально
информация от продвинутого аккумуляторщика:
Я решился написать эту статью с целью собрать в одном месте ранее написанные мои посты об особенностях использования свинцовых аккумуляторов, и развенчанию особенно вредных мифов об их использовании и восстановлении.
Статья написана на основании собственных исследований как литературы так и отдельных тестовых ячеек в хим.лаборатории.
Я повторял и повторяю еще раз: свинцовый аккумулятор мало чем изменился за последние 100лет, он постоянно подвергается варварскому отношению со стороны «потребителей», которое с успехом выдерживает 😊 потому что обладает практически идеальной хим. схемой. Но об этом ниже.
( заранее извиняюсь за «многабуков». ) 😀
Итак, как это ни банально но начнем с азов.
Примерно в 1859-1860 годах в лаборатории Александра Беккереля, работал в качестве ассистента Гастон Планте. Молодой человек решил заняться улучшением вторичных элементов, чтобы сделать их надежными источниками тока для телеграфии. Сначала он заменил платиновые электроды «газового элемента» Грове свинцовыми. А после многочисленных экспериментов и поисков вообще перешел к двум тонким свинцовым пластинкам. Он их проложил суконкой и навил этот сэндвич на деревянную палочку, чтобы он влезал в круглую стеклянную банку с электролитом. Далее подключил обе пластины к батарее. Через некоторое время вторичный элемент зарядился и сам оказался способен давать достаточно ощутимый постоянной ток. При этом, если его сразу не разряжали, способность сохранять электродвижущую силу оставалась в нем на довольно продолжительное время. Это было настоящее рождение накопителя электрической энергии, или аккумулятора.
Самое интересное, что до сих пор самые мощные(по отдаваемому току и принимаемому току зарядки) свинцовые аккумуляторы это аккумуляторы фирмы «Оптима», и построены они тоже по «спиральному» принципу! . история до сих пор ничему не учит остальных производителей 😞
Потом было обнаружено, что если заряженный первоначально прибор(см. рис выше) разрядить, затем пропустить через него ток в обратном направлении, да еще проделать эту операцию не один раз, то увеличивается слой окисла на электродах и емкость вторичного элемента возрастает. Этот процесс получил название формовки пластин и занимал у изобретателя Камилла Фора около трех месяцев.
После Парижской выставки 1878 года Фору пришла идея нового метода формовки пластин. Он попробовал заранее покрывать их оксидом свинца, свинцовым суриком. При зарядке сурик на одной из пластин превращался в перекись, а на другой соответственно раскислялся. При этом слой окисла приобретал очень пористое строение, а значит, площадь его поверхности существенно увеличивалась. Процесс формовки проходил значительно быстрее. Аккумуляторы Фора при том же весе запасали значительно больше электрической энергии, чем аккумуляторы Планте. Другими словами, их энергоемкость была выше. Это обстоятельство привлекло к ним большое внимание электротехников.
Технология «намазных пластин» современных аккумуляторов даже сейчас, спустя более 100 лет, остается такой-же. 😞 Кто не верит — читаем книгу:
М. А. Дасоян, В. В. Новодережкин, Ф. Ф. Томашевский
ПРОИЗВОДСТВО ЭЛЕКТРИЧЕСКИХ АККУМУЛЯТОРОВ
http://publ.lib.ru/ARCHIVES/D/. ).%5Bdjv%5D.zip
Немного химии.
С точки зрения хим. динамики свинцовый аккумулятор(далее СА) представляет обратимую систему, и именно обратимый гидроэлектрический элемент. Восстановление свободной энергии такого элемента выражается накоплением на электродах продуктов электролитического распада. В теории гальванических элементов такое накопление, вторичный эффект эл.-хим. процесса, носит название поляризации. Вредное в обычных элементах, это побочное явление положено в основу службы СА, называемых поэтому вторичными, или поляризационными, элементами. В принципе, всякий СА состоит из одного электролита, содержащегося в некотором баке, и двух электродов с клеммами. Положительный электрод называется анодом, отрицательный—катодом (в американской литературе катод — положительная пластина, анод — отрицательная). Аккумуляторы различаются между собою химической природой электролита и электродов, формой и строением электродов, устройством бака и т. д.
Описание физ.-хим. процессов в СА
Разрядка и зарядка СА. характеризуются графиком, при чем как разрядная, так и зарядная кривые претерпевают три последовательные стадии
Рекомендуемый График заряда батареи после глубокого разряда.
Графики разрядных характеристик при различных скоростях разряда
Стадия I: Занимает короткое время.
Зарядка: Сначала разность потенциалов быстро поднимается над значением 2V, соответствующим плотности электролита, а затем падает до 2,1V.
Разрядка: разность потенциалов очень быстро падает до 1,9 V.
Стадия II: Занимает наибольшую часть.
Зарядка: Разность потенциалов медленно возрастает, приблизительно до 2,2V.
Разрядка: Разность потенциалов медленно убывает, приблизительно до 1,85V.
Cтадия III: Занимает сравнительно небольшое время.
Зарядка: Разность потенциалов довольно быстро возрастает до 2,5—2,6V.
Разрядка: Разность потенциалов быстро падает, при чем кривая претерпевает изгиб и стремится к нулю (см. выше графики разряда — зависит от тока разряда!)
Этим трем стадиям соответствуют характерные видимые явления: в заряженном СА. катод имеет серо-металлический вид и состоит из губчатого свинца,тогда как анод покрыт перекисью свинца Pb2O5 интенсивного черного цвета, нестойким, сильно окисляющим веществом с значительной электропроводностью. Внезапное понижение стадии I разрядки происходит от уменьшения концентрации кислоты в порах активной массы СА, после чего концентрация выравнивается диффузией частиц кислоты в электролите.
Это очень важный момент, который надо понимать — из-за того что в СА применяется жидкий электролит, и толщина «намазки» пластин существенна, самым идеальным способом зарядки(да и разрядки!) СА была-бы пульсирующая зарядка, т.е. с применением ШИМ, а лучше «медленно-пульсирующего» типа — когда за плавным нарастанием импульса следует пауза, в течении которой происходит «усвоение» порции энергии(идут.хим процессы) и выравнивается плотность электролита(т.е. подается к материалу пластин новая порция серной кислоты из раствора).
Аналогично и для разрядки — мы знаем что если «дать отдохнуть» СА (сняв с него всю нагрузку) то напряжение на СА повышается и с него можно еще получить энергии. Обьяснение аналогичное: выравнивание плотности электролита, т.е. подача кислоты к материалу пластин за счет диффузии.
Стадия III разрядки связана со вторичным уменьшением концентрации кислоты. В разряженном CА. анод состоит из двуокиси свинца РЬО2, вещества бурого цвета, с удельным сопротивлением в 22 раза большим, чем у перекиси свинца Pb2O5. Катод состоит из недокисного сернокислого свинца Pb2SO4, вещества темносерого, почти черного цвета, обладающего значительною электропроводностью и весьма нестойкого. Удельный вес электролита падает от уменьшения концентрации кислоты как раз в количестве, потребном для образования на катоде недокисной сернокислой соли. Именно поэтому, оставленный в бездействии незаряженный СА. гибнет («сульфируется», «сульфатируется» 😛, при чем и катод и анод покрываются окисным сернокислым свинцом PbSO4, веществом белого цвета, электронепроводящим и стойким.
Если оставить батарею в разряженном состоянии, сульфат свинца начинает растворяться в электролите до его полного насыщения, а затем выпадает назад на поверхность пластин, но уже в виде крупных и практически нерастворимых кристаллов. Они откладываются на поверхности пластин и в порах активной массы, образуя сплошной слой, который изолирует пластины от электролита, препятствуя его проникновению вглубь. В результате большие объемы активной массы оказываются «выключенными», а общая емкость батареи значительно уменьшается.
Почему батарея из нескольких АКБ выходит из строя и неравномерно заряжается ?
Это то что происходит внутри АКБ.
желтым — выделены «разряженные намазки». Зеленым — заряженные, в которых все вещества прореагировали.
Смотрите и думайте.
Ход реакций, по классческому учебнику» таков:
на катоде. . . . Pb+H2SO4+O ->PbS04+H20 I
на аноде . . Pb2SO4+H2SO4+O -> 2PbSO4+H2O II
Это и есть процесс сульфации или сульфатации, разрушающий электроды оставленного незаряженным СА. 😞
Но. «Теория двойной сульфатации» говорите ? 😛
ну так вот еще пара кусочков «старого знания» — все эти реакции
(в том числе 20(!) неэлектродных, которым не нужна кислота!), протекают внутри Свинцового Аккумулятора,
и каждая из них вносит свою лепту в процессы:
Кому верить ? 😊
. мои опыты и построенные на их базе «Умные зарядки» говорят о том что надо верить этим двум картинкам.
При сульфатации(сильном разряде) концентрация кислоты опять падает. При зарядке СА с пластинами, не подвергшимися выпадению кристаллов, катод вновь принимает серо-металлический цвет, анод чернеет, а концентрация электролита повышается. Зарядные и разрядные кривые СА. не совпадают между собой, и площадь между ними выражает потерю энергии на цикл зарядки и разрядки. Однако совершенное смыкание кривых доказывает, что в СА не происходит побочных реакций и что его можно рассматривать как элемент с почти совершенной обратимостью!
Но не все так гладко, как пишет нам учебник.
С момента изобретения свинцового кислотного аккумулятора и разработки в 1882 г. английскими исследователями Gladstone и Tribe химической теории, описывающей токообразующие реакции, протекающие на электродах свинцового аккумулятора при его разряде и заряде, известной как теория «двойной сульфатации», и до настоящего времени предпринимались неоднократные попытки пересмотреть эту теорию, предложить иной механизм протекания реакций (см. выше таблички с 63 реакциями)
Причины такого положения заключаются в том, что, не взирая на общее признание исследователями теории «двойной сульфатации» наиболее точно теоретически описывающей термодинамические процессы в свинцовом аккумуляторе, до настоящего времени существуют противоречия в количественной оценке веществ, участвующих в токообразующих реакциях, оценке состава веществ, образующихся па положительном электроде при разряде аккумулятора, а также в описании механизма протекания реакций на электродах аккумулятора. По многим вопросам у исследователей отсутствует единая точка зрения. Отдельные вопросы теории аккумулятора вообще подробно образом не освещены.
Теорию свинцового аккумулятора нельзя считать завершенной.
Так, например, согласно теории «двойной сульфатации» продуктом токообразующей химической реакции при разряде аккумулятора на положительном электроде является нерастворимое химическое вещество PbSO4 , осаждаемое на поверхности активной массы в количествах, обеспечивающих отдачу аккумулятором номинальной емкости.
Авторы «Учебников» пишут, не моргнув глазом, о «двойной сульфатации», но при таком механизме протекания токообразующей реакции уже при разряде аккумулятора на 1А·ч емкости поверхность его положительных электродов должна быть покрыта не менее чем 2 монослоями сульфатов свинца PbSO4, размер кристаллов которых сопоставим с диаметром пор в активной массе.
В результате этого свободный доступ молекул кислоты из состава электролита через поры к активной массе положительного электрода затруднится, в связи с чем химическая реакция разряда должна будет прекратиться, чего на самом деле не происходит.
Полученная при расчётах интенсивность сульфатации электродов свинцового аккумулятора при его разряде на величину номинальной емкости оказалась слишком высокой, составляет десятки и сотни монослоев, что свидетельствует о том, что поверхностный процесс зарядообразования, протекающий согласно общепринятой теории «двойной сульфатации», не обеспечивает фактическую ёмкость реального аккумулятора!
То есть: в случае протекания химических реакций при разряде в свинцовом аккумуляторе в соответствии с теорией «двойной сульфатации» при снижении емкости на величину, не более 1 – 2% от номинальной, происходил бы его полный разряд.
Таким образом, полученные результаты исследования элементного состава активной массы положительных электродов аккумулятора разными учеными ставят под сомнение справедливость предлагаемого теорией «двойной сульфатации» механизма протекания электродного процесса на положительном электроде при разряде аккумулятора.
Следовательно, теория «двойной сульфатации» не полностью объясняет протекание процессов зарядо- и токообразования, саморазряда в свинцовом кислотном аккумуляторе и требует уточнения.
Теперь давайте поговорим немного о доставшей уже всех теме «ШИМ большими токами разрушает свинцовую АКБ» 😊
Согласно исследованиям Battery Council International, 84% свинцово-кислотных батарей выходят из строя из-за сульфатации. Сульфатация является еще более остной проблемой в солнечных энергосистемах, потому что вероятность полного заряда в таких системах сильно отличается от традиционного заряда АБ. Увеличенные периоды недозаряда АБ в солнечных энергосистемах приводят к коррозии решетки, а положительные пластины аккумуляторов покрываются кристалами сульфатов.
Широтно-импульсная модуляция тока заряда может предотвратить образование отложений сульфатов, помогает преодолеть резистивный барьер на поверхности электродной сетки и пробить коррозию на переходах. В дополнение к улучшенному КПД заряда и увеличенной емкости, существуют убедительные доказательства того, что такой режим заряда может восстановить емкость АБ, которая «потерялась» со временем при работе АБ в фотоэлектрической системе. Некоторые результаты исследований приведены ниже.
В 1994 CSIRO, ведущая исследовательская группа в Австралии [1], опубликовала статью, в которой указывается, что пульсирующий ток заряда «позволяет восстановить емкость элементов, работавших в циклическом режиме». Процесс сульфатации замедляется, а внутренние слои коррозии становятся тоньше и разделяются на «островки». Электрическое сопротивление уменьшается и емкость увеличивается. Вывод статьи в том, что пульсирующий ток заряда «может привести к восстановлению емкости аккумуляторной батареи.»
Другая статья, опубликованная Sandia National Labs в 1996 году [2], приводит данные по тестирования герметичных аккумуляторов, которые потеряли более 20% своей емкости. Обычный заряд постоянным током не мог восстановить потерянную емкость АБ. Затем батарея была заряжена с использованием ШИМ контроллера, что привело к «восстановлению большей части потерянной емкости АБ.»
Наконец, Morningstar, провели тесты по восстановлению емкости АБ. Прилигаемый график [3] показывает, что аккумуляторная батарея восстановиля большую часть потерянной емкости после заряда при помощи SunLight контроллера. После теста, солнечная система освещения в течение 30 дней практически не обеспечивала освещение, так как система отключалась по защите от перезаряда каждую ночь. Аккумуляторная батарея была очень старой и подлежала утилизации. Затем, нагрузка стала работать дольше каждую ночь, что отражено на графике. В течение последующих 3 месяцев емкость АБ постоянно возрастала. Этот тест продолжается в Morningstar.
Позднее было проведено исследование контроллеров с ШИМ, которое доказало, что контроллеры повышали восприимчивость АБ к заряду именно вследствие использования широтно-импульсной модуляции тока заряда. Контроллеры MorningStar SunSaver позводили даже увеличить эффективность заряда АБ на 2-8% даже по сравнению с контроллерами, которые поддерживали постоянно высокое напряжение на АБ.
Литература:
1. Lam, L.T., et al, ‘Pulsed-current charging of lead/acid batteries-a possible means for overcoming premature capacity loss?,’ CSIRO, Australia, Journal of Power Sources 53, 1995.
2. Hund, Tom, ‘Battery Testing for Photovoltaic Applications,’ Sandia National Laboratories, Albuquerque, NM, presented at 14th NREL Program Review, Nov. 1996.
3. Morningstar test results, 1999. http://www.morningstarcorp.com. 0Why%20PWM1.pdf (реальные тесты для особо неверующих 😊
Что здесь правда или похоже на правду ?
Правда то что пульсирующее напряжение заряда(разряда) очень хорошо ложится на химию процесов в СА — т.е. в паузах между импульсами идет диффузия электролита.
Неправда тут в том что не все АКБ удастся восстановить таким способом 😞 старый анекдот про «поздно пить Боржоми когда почки отвалились» 😊 т.е. если вы гоняете СА «от конца до конца» то вы тем самым расшатываете частицы намазных пластин, тем самым способствуете осыпанию состава пластин вниз банок 😞 Это характерно для «наливных» СА — т.е. «стартерного типа» , где сепаратор, как и 100лет назад, состоит из простых пластин с дырочками погруженных в кислоту 😊. В аккумуляторах AGM технологии осыпания пластин нет, потому что они жестко схвачены стекломатами. Следовательно, при бережном обращении, СА AGM типа могут эксплуатироваться во много раз дольше чем СА со «свободным»(плещущимся) электролитом. Но это при условии НЕДОПУЩЕНИЯ сульфатации.
Про аккумуляторы AGM технологии я писал вот тут:
http://electrotransport.ru/ussr/index.php/topic,1950.0.html
Восстановление «УПСовых» аккумуляторов — смотрите там-же.
Есть для электромобилистов еще одна хорошая новость — компания Варта начала выпуск стартерных СА по технологии AGM емкостью до 100Ач:
http://www.bat.by/product.php?id=84
и вместе с этой новостью мы подошли к еще одному важному вопросу:
Есть-ли разница в применении для электротранспорта «стартерных» и «тяговых» СА?
Производители СА нам врут 😞 Ведь по идее эти СА должны чем-то отличаться, но на практике, мне лично пришлось позаглядывать внутрь разных СА разных предназначений от разных производителей — так вот — обещанное правило «у тяговых СА пластины толще» не работает 😞
Внесем ясность — с точки зрения Химии процессов, вы НИГДЕ в литературе не увидите разных характеристик — т.е. отдельно для тяговых и отдельно для стартерных. Химия-то внутри одна! В чем-же разница ? в том что (по науке) стартерные СА должны разрабатываться с учетом отдачи больших токов (сотни ампер), а тяговые нет — они должны отрабатывать меньшие токи но более длительный период.
И вот тут-то и начинается «минное поле вранья». Рассмотрим плюсы и минусы.
Более толстая намазка при тех-же токосьемных электродах, дает бОльшую емкость СА. Но при этом у СА «свободного электролита» способствует большему разрушению намазки пластин 😞 из-за того что технология по прежнему 100 лет не меняется 😞 — вся активная паста держится только за счет своих свойств как «застывшей замазки». Читаем книгу М. А. Дасоян, В. В. Новодережкин, Ф. Ф. Томашевский — ПРОИЗВОДСТВО ЭЛЕКТРИЧЕСКИХ АККУМУЛЯТОРОВ и плачем.
Более толстая намазка также способствует более длительному времени «отдыха» СА, так как в толстых массах пластин процессы диффузии идут медленнее 😞
Более тонкая намазка при тех-же токосьемных электродах, дает бОльшую способность отдачи токов от СА. При этом гораздо меньше время «отдыха» (диффузия лучше) и гораздо более доступны хим.элементы пластин — я видел «польские нонейм» АКБ у которых количество пластин было раза в полтора больше и они были тоньше чем у подобных-же стартерных — так вот «ударный разряд» они держали гораздо лучше чем «классика».
. самое интересное что если заклеить все надписи в СА и дать вам фонарик заглянуть в банку СА — то вы в 90% случаев не сможете отличить стартерные СА от тяговых 😞
А давайте теперь все что я написал выше суммируем и попытаемся представить себе «идеальный СА» имеющий не ниже 3000 циклов 😊 и быстро отдающий и быстро принимающий токи в сотни ампер, при этом имеющий отдачу энергии в 3-4 раза выше при том-же весе как аналогичный «классический стартерный». Фантастика ? НЕТ — это реальность!
Что мешает долгой жизни СА ? Разрушение пластин-токоотводов(из-за изменения плотности намазки в процессе циклирования) плюс сульфатация.
Что мешает растворению «сульфат. слоя» ? низкая его электропроводимость.
Что даем нам до 70% лишнего веса СА? толстые токоотводные пластины СА из свинца. (в AGM аккуме 12Ач CSB активная масса составляет до 20-25% от общего веса СА — проверено мной лично при разборках этих СА. )
Что в итоге ? В итоге видим картинку «идеального СА»:
😛 . и вспоминаем «Оптиму».
Если электроды сделать не из свинца а из легкого проводящего материала (например карбоновая ткань), если электролит впитать в «стекломат» или в новейшие материалы, которые способны впитывать больше своего веса, если состав активной массы сделать гранулярным, как в ЛитийФосфатных, чтобы каждая «гранула» была окружена проводимой оболочкой из графита.
То после сворачивания всего этого в рулон — как на картике :0 мы получим идеальный СА, который будет в состоянии отдавать сотни ампер продолжительное время, не разрушаясь и не «отдыхая», и не боясь сульфатации.
. и мои личные опыты говорят о возможности создания такого СА.
Спасибо за внимание ! :ax:
Всем кто все еще не понял «что там внутри» — рекомендую старую книгу:
Н.Ламтев. Самодельные аккумуляторы. Москва: Государственное издательство по вопросам радио, 1936 год.
Брошюра «Самодельные аккумуляторы» написана простым и понятным для всякого грамотного языком и содержит все главнейшие материалы и сведения, относящиеся к практике изготовления, ремонта и эксплоатации простейшего типа свинцовых аккумуляторов.
http://retrolib.msevm.com/energetika_1.html
. кстати — из нее вы узнаете что технологии AGM и «гелевого(силиконового) электролита» была изобретена гораздо ранее мировых войн 😛
ну и чуть-чуть саморекламы 😊
http://electrotransport.ru/ussr/index.php/topic,762.0.html
я до сих пор веду работы по применению полученных знаний 😊 в автоматических зарядных устройствах для СА.
«Итак, продолжим тему.
Теперь я хочу остановиться на теме зарядки Свинцовых Аккумуляторов(далее СА), и процедурах их «лечебных циклов» а также «восстановления».
Есть такая наука — ХИМИЯ. И все что происходит в СА подчиняется законам Химии. Все «умные советы бывалых» которые не ложатся на химию — вредны по определению.
. а вот за такие «советы» http://oppozit.ru/article416.html — надо просто голову откручивать :aq:
Восстановление после сильной сульфатации.
Лежит вот на полке(или в сарае) СА. несколько лет лежит. выбросить ?
Хранение в «полном разряде», как и постоянные «сверх-полные разряды» приводят к образованию зерен сульфатов, которые разрушают «активную намазку = активное вещество». И рост кристаллов сульфатов приводит также к выводу из реакции веществ и увеличению сопротивления.
Но самое интересное — что эти вот «переходы» способствуют разрыхлению активной массы, что есть хорошо для химии.
Вот как выглядит покрытая сульфатацией пластина классического СА:
светлые пластины это сульфатация.
Как разрушить кристаллы сульфатов ? . самое лучшее — не доводить до них. а если они есть — то надо их растворять неглубокими циклами заряд-разряд. Но крупные кристаллы вы не полечите они имеют более высокое сопротивление и плохо «работают». так что речь может идти только о неполном восстановлении. Вывод: не допускайте глубоких разрядов!
Как грамотно произвести работы по десульфатации ?
Есть два способа — первый это купить мою умную зарядку-автомат 😊 потому что у них есть специальный режим для таких случаев. В этом режиме зарядка дает импульсы тока примерно 1А напряжением 14.5В с переменной скважностью, зависящей от степени разряда (напряжением на СА) СА. Т.е. если на СА например 10В то будет импульс с частотой следования примерно 0.5-1Гц. При этом продолжительность импульса вдвое меньше паузы или равна ей. В процессе повышения напряжения на СА до 12В частота следования импульсов (а в некоторых зарядках — продолжительность(скважность) импульса тока) увеличивается пропорционально, и с 12В уже идет просто зарядка постоянным током.
Также известен способ восстановления СА батарей асимметричным током (при соотношении зарядной и разрядной составляющих тока 10:1 и отношении длительностей импульсов этих составляющих 1:2. Но этот метод обычно делается на частотах 50Гц(сеть 220В) 😞 и я его не рекомендую — так как 50Гц это «сильно быстро» и будет лишний нагрев СА. Хотя само соотношение «зарядка:нагрузка» в 10:1 (по току) я рекомендую применять для низких частот (0.5-1Гц).
Второй способ — это собрать из подручных средств простую схему, в которой с частотой 0.5-1сек будет происходить переключение СА с зарядки на разрядку.
Самое простое — использовать «реле поворотов» от автомобиля 😊 и лампочку в качестве нагрузки. Но следует помнить что «реле поворотов» недолговечно да и «клацает» громко — так что длительная работа «простой схемы» под вопросом.
пример реализации есть у нас на форуме: http://electrotransport.ru/uss. 51820#msg251820
Соотношение «зарядка:нагрузка» в 10:1 (по току) я рекомендую применять и в этом случае.
Процедура тренировки-десульфатации которую я рекомендую:
(прежде чем ее делать прочтите мой пост#4: http://electrotransport.ru/ussr/index.php/topic,1950.0.html )
Собрать схему «с реле и лампочкой» (как самый простой и доступный пример), для циклирования СА — так чтобы подавать постоянное напряжение ХХ в 18-20В(под нагрузкой на ваш СА оно должно падать до 14.5В) с током не более 0.5С для 7-10Ач АКБ и 0.05С для 50-120Ач вперемешку с подачей нагрузки(лампочки). Лампочку(т.е. нагрузку) выбирать из расчета 20 часового разряда для вашего СА. (лампочку параллельно на клеммы СА, а «реле поворотов» в разрыв источника питания и СА с лампочкой).
Большинство производителей СА рекомендуют 20 часовой разряд токами в 0.05С до 1.8В/элемент (т.е. до 10.8В на 12Вольтовом СА, измеренные под нагрузкой, или не ниже 12В без нагрузки). 10-и часовой разряд будет примерно при 0.1С.
Применение этой схемы при 10 часовой тренировке дает 1:1 «нагрузка:пауза» (немного не то что я писал ранее но зато этого 1:1 очень просто достичь) и способствует более полному использованию хим.веществ, потому что в паузах выравнивается плотность электролита.
Ну а для тех кто «дружит с паяльником» — я уверен не составит труда спаять простой мультивибратор 😊 на двух транзисторах или микросхеме, и с него производить «лечебные циклы».
Как у знать что «лечебные циклы» закончились ?
Вопрос важный. при применении «умных зарядок» они сами контролируют напряжение. Но в случае «реле и лампочки» я просто рекомендую не злоупотреблять процессом и ограничить время тренировки 10 часами при соблюдении непревышения токов (см. выше). После такой «тренировки» устройте СА 10 или 20 часовой разряд до 10.8В(под нагрузкой) — и посмотрите что получилось — если емкость не повысилась — то значит у нас не сульфатация а разрушение пластин 😞 и «Боржоми не помогло».
Если в процессе тренировки было «кипение» электролита — то добавьте дистиллата в банки СА. как именно описано тут:http://electrotransport.ru/ussr/index.php/topic,1950.0.html
Просто разрядку 10-20 часовым циклом можно делать и с применением «реле поворотов» 😊 при этом вы просто способствуете более полному использованию хим. веществ СА — потому что в паузах вы позволяете работать диффузии.
ТОЛЬКО НЕ забывайте что нельзя разряжать 12В СА ниже 10.8В .
Следует помнить про «почки и Боржоми», т.е. я не рекомендую возлагать большие надежды на «волшебное восстановление» старых автомобильных СА — там на 80% вероятность разрушения пластин и их осыпание — так что все что вы сможете это только восстановить емкость тех обрывков пластин которые еще висят на токоотводах. 😞
Для малогабаритных AGM СА (УПс-овых) осыпание пластин не страшно но страшно их разрушение от постоянного перезаряда, так что если вы вскрыли крышки (см. методику тут: http://electrotransport.ru/ussr/index.php/topic,1950.0.html ) то убедитесь что внутри ничего лишнего не болтается.
Идем дальше.
Постоянный «маленький подзаряд» токами до 300мА при 13.5В — как это делают УПСы и прочие «умные советчики», приводит к тому что когда кончается активная масса(губчатая) внутри акка — то начинается реакция в его электродах. т.е. свинец токоотводов на (+) становится коричневым(PbO2) а на (-) стает губчатым. Таким образом, при постоянном перезаряде, мы получаем разрушение токоотводов + «кипение» электролита с выделением водорода и кислорода, что приводит к увеличению концентрации электролита, что опять способствует разрушению электродов 😞
Я писал про акки из УПСа после 3 лет — (+)пластины рассыпаются в порошок.
В старых умных книжках есть советы как из свинцовой пластины сделать СА для «анодной батареи» — так вот наработка «активной массы» идет из самого материала пластин 😞 только вот циклов там надо много — ну или постоянно «кипятить» — это как раз наш случай — перезарядка переводит свинец токоотводов в порошок оксида свинца.
Общий вывод: береги честь смолоду, а свинцовый акк с момента покупки!
Нельзя разряжать в ноль, и нельзя перезаряжать — тогда вы работаете только с «активной массой» и не допускаете разрушения пластин. Аминь.
Надо доливать воду — хотя-бы раз в год. Вода все равно разлагается, а водород улетучивается даже сквозь материал баков.
Отрывок из учебника:
.
Напряжение в процессе разряда
Номинальное напряжение свинцового стационарного аккумулятора любой емкости принято считать равным 2 в. Это наименьшее допускаемое напряжение на зажимах полностью заряженного аккумулятора в течение первого часа разряда десятичасовым режимом при плотности раствора ск 1205±5 кг/м3 и температуре его +25’С. Предельное напряжение, до которого разрешается разряжать
аккумуляторы при температуре раствора ск +25? С, составляет по ГОСТ
825—61 для режимов разряда не короче трехчасового = 1,8 в, а для более коротких режимов (включая 15-минутный)—1,75 в. В действительности у исправных аккумуляторов напряжение в конце разряда часто бывает несколько выше.
Указанные предельные значения напряжений, до которых можно
разряжать аккумуляторы, установлены опытным путем. Они выбраны с
таким расчетом, чтобы не вся активная масса превращалась при разряде в сернокислый свинец, так как это вызвало бы чрезмерную сульфатацию пластин.
Кроме того, глубокие разряды, которые сопровождаются существенным изменением объема активной массы, могут привести к частичному отделению и выпаданию активной массы и вызвать коробление пластин. Кроме того, эффект от разряда до более низких напряжений при нормальном десятичасовом разряде и более коротких режимах разряда очень мал. После предельно допустимого значения (1,8 или 1,75 в) напряжение резко идет на убыль и может быстро достигнуть таких малых величин, которые непригодны для практического их использования. Кроме того, величина получаемой при этом добавочной емкости невелика.
В конце хотелось-бы посоветовать тем кто не имеет средств на покупку новых СА — найдите в Вашем городе фирмы которые занимаются компьютерной техникой и УПс-ами. Поознакомтесь с ними и договоритесь чтобы они не выбрасывали старые УПсовые СА а отдавали их вам 😊 . можете даже выкупать «не полностью убитые» СА по небольшим ценам.
из моей практики — примерно 30% AGM СА удается восстановить. Правда не всегда до 100% емкости но до 80% уж точно. А это пару лет вашей езды на электровелосипеде. :ay:
Спасибо за внимание!
Lev007
Вот сколько лет могут хранится сухозаряженные свинцово-кислотные аккумуляторы?
Источник