Магниевый аккумулятор своими руками
Евросамоделки — только самые лучшие самоделки рунета! Как сделать самому, мастер-классы, фото, чертежи, инструкции, книги, видео.
«Вечная» магнивая батарейка своими руками
Подобные источники тока незаменимы в различных автономках – они конструктивно очень просты, в них нечему ломаться, они бесшумны, а «топливо» — легкое и безопасное. Фактически нужны только анодные пластины и соль – воду можно взять хоть из лужи. А в случае использования морской воды не требуется даже соль – хватит той, что уже растворена в воде.
Комплект для батареи.
Стержень из магния минусовый. Длина 45мм, диаметр 20мм.
Медная гильза. Длина 60мм, диаметр 25мм.
Элемент в разобранном виде.
Крепление минусового вывода.
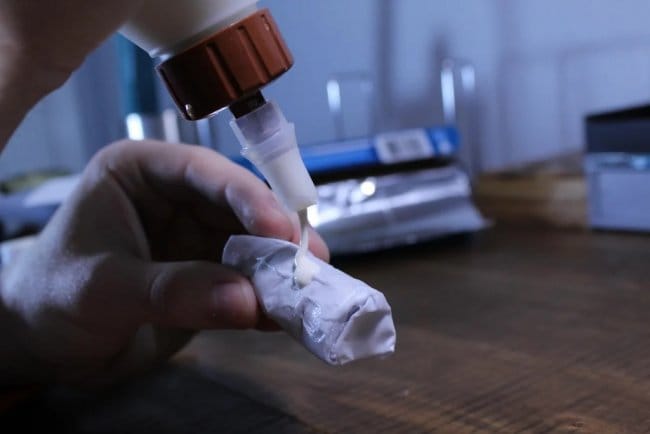
Ткань в качестве сепаратора. Сборка элемента.
Электролит обычная, солёная вода.
Элемент в сборе.
Напряжение одного элемента 1,25 Вольта.
Источник тока работает, пока аноды полностью не растворятся. После чего нужно просто установить новые аноды, вылить отработанный электролит и залить соленую воду снова. Причем, выливать электролит можно прямо в реку или озеро – при использовании алюминиевых или магниевых анодов он экологически безвреден! Нечто подобное люди даже… употребляют внутрь – аналогичный состав у альмагеля, известного желудочного лекарства!
Смотрите также:

Делайте самоделки своими руками как мы, делайте лучше нас!
Источник
Самая дешевая батарейка
Умелец создал батарейку, которая работает от обыкновенной воды из под крана (электролит). Все началось после того, как он начал экспериментировать с картофелиной в качестве электролита, а потом решил заменить ее на воду. И результат проверки работы самой дешевой батарейки превзошел его ожидания.
Система электродов: первый электрод – брусок из магниевого сплава, а второй – кусок угля. Автор использовал уголь от контактных троллейбусных щеток. Заметим, что он не играет в этом устройстве роль катализатора. Два элемента соединены последовательно. Каждый из них выдает 1,5 вольта, а в совокупности на выходе напряжение в 3 вольта достаточно для питания светодиода, рабочее напряжение которого 2,5 вольта. Эти пары электродов помещаются в стаканчики и в них наливается вода.
Почему использованы такие материалы? Магниевый сплав и графит (углерод) имеют большую разницу электрохимических потенциалов.
Лампочка загорается без каких-либо дополнительных манипуляций. Особенностью генерации электричества при работе этой дешевой батарейки является выделение из воды водорода рядом с электродом, который изготовлен из магниевого сплава. Два стакана могут обеспечить работу такой батарейки в течение суток. Угольный электрод (электроды) нужно максимально сблизить с магниевым, для этого следует проложить между ними прокладку, пропускающую ионы, например, бумагу.
Автор этой батарейки объясняет механизм ее работы так. “Электрон-отрицательно заряженная частица. Его аналог с положительным зарядом называется позитрон. Здесь идет обмен плюс и минус ионами. Расходуется магний и вода. Уголь сохраняется. Причем, магниевый электрод покрывается тончайшей окисной пленкой, выделяя из воды водород.”
Если есть трудности в поиске магниевого сплава, автор водяной батарейки рекомендует использовать алюминий, например, уголок. Напряжение на выходе с одной батарейки исходного размена будет уже 1 вольт, поэтому нужно увеличить площадь алюминиевого электрода и уменьшить расстояние между углем и пластиной с помощью прокладки из бумаги.
После добавления воды на вторые сутки работы мощности батарейки хватит уже на меньшее время. Однако если регулярно по необходимости чистить шкуркой от очень тонкого слоя окисла поверхность пластины из магниевого сплава, то генератор каждый раз будет работать как новый. Заработает как новая. Второй электрод (угольный) зачищать необходимости нет. С учетом того, что слой окисла очень тонкий, батарейка практически “вечная”.
Надеемся, что кто-нибудь проверит эту идею и напишет о результатах в комментариях.
Первая батарейка на картофелине, которая послужила отправной точкой для водяной – ниже.
2 комментария
Проверил работу водной батарейки, но так как у меня магниевая лента узкая и тонкая всего 3мм шириной 0,2 мм толщиной, на долго не хватило.
это же вполне обычный гальванический эллемент, такие умели делать ещё в конце XIX и начале ХХ века, грубо говоря – самая обыкновенная батарейка, но с тем отличием, что эта батарейка имеет возможность повторного использования и “дозаправки”
Источник
Как сделать аккумулятор своими руками
Есть множество способов сделать самодельные батарейки. К сожалению, большинство самодельных аккумуляторов либо бесполезны, либо потенциально опасны и сложны в изготовлении. Батареи из лимона и картофеля, как правило, очень слабые и требуют в качестве материала скоропортящегося органического растительного материала, в конструкцию свинцово-кислотных аккумуляторов входят высокотоксичные и едкие химикаты и т.д.
Эта батарея сделана из очень простых и доступных материалов, и обладает достаточной мощностью для работы устройств. Когда традиционные батареи недоступны эта батарея будет отличным аварийным источником электроэнергии. Кроме того, ее можно легко перезарядить практически от любого источника постоянного тока, она очень легкая и, в отличие от более распространенных алюминиево-воздушных батарей, не требует воздушного потока для работы.
Шаг первый: дизайн и теория
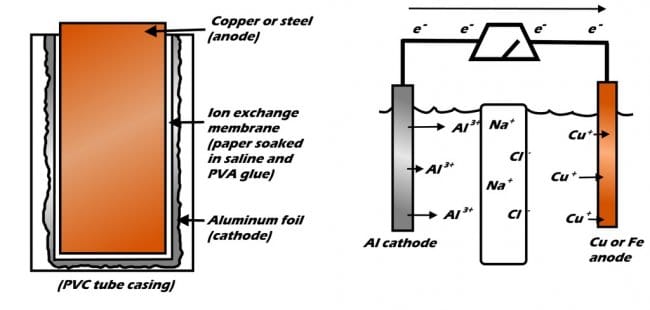
Принцип работы батарей основан на химической реакции, известной как окислительно-восстановительная реакция. В окислительно-восстановительной реакции одно вещество окисляется (теряет электрон), а другое восстанавливается (приобретает электрон). Довольно просто. Любая батарейка устроена схожим образом, в ней обязательны три элемента, между которыми происходит химическая реакция, в результате которой возникает электричество: электроды — анод, катод, и электролит.
В этой алюминиево-металлической батарее две половины батареи пропитаны физиологическим раствором и разделены специальной мембраной, пропускающей только ионы натрия и хлора. Алюминий с одной стороны начинает окисляться, в то же время как медь или сталь на противоположной стороне пытаются остаться стабильными.
В принципе любая батарейка или аккумулятор это две металлические пластины, помещенные в специальное химическое вещество – электролит. Одна пластина подключается к плюсу, вторая к минусу. Пока батарею не трогают, на ней остается стабильное напряжение, например, 3 или 9 В. Стоит подключить к батарейке нагрузку, лампочку, вентилятор, как от плюса к минусу потечет ток. Напряжение начнет падать и сразу же начнется окислительно-восстановительная реакция. Электроны начнут перетекать с отрицательной (-) пластины обратно на положительную, поддерживая тем самым разность потенциалов между ними.
Реакции бывают обратимыми (аккумулятор) и необратимыми (батарейка). Т.е. в батарейке реакция необратимая и ее нельзя зарядить, а в аккумуляторе обратимая и он заряжается. Если подключить аккумулятор к зарядному устройству, ток внутри него начинает течь в обратном направлении, то есть – от «+» к «-». И реакция в электролите также начинает идти в обратном направлении. В результате, продукт реакции разлагается на исходные вещества. Аккумулятор «заряжается»
Конечно, этот процесс не бесконечен и наступит момент, когда одна из пластин разрушится и химическая реакция больше не сможет проходить.

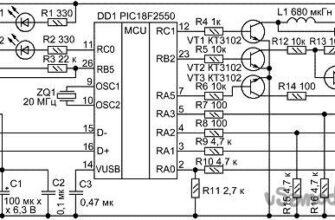
Шаг пятый: зарядка и проверка
Аккумуляторная батарея готова, но ее нужно зарядить. Можно использовать практически любой источник постоянного тока, если ток не слишком велик (до 5 А). Чтобы зарядить аккумулятор, нужно подключите анод к плюсу зарядного устройства, а катод к минусу. Во время зарядки ток начнет уменьшатся по мере того, как батарея набирает заряд. Это является хорошим признаком, и говорит о том, что батарея работает правильно. После зарядки нужно проверить аккумулятор мультиметром. Используя медный анод, мастер получил максимальное напряжение 1,44 В после скромного цикла зарядки. Максимальный ток, который он получил от батареи, был большим для такой самодельной батареи — 1.2 А. Для сравнения, лимонные или картофельные батареи обычно выдают в лучшем случае всего несколько миллиампер. Коммерческая батарея D-cell может выдавать ток более 5А.
Так же мастер провел тест, в котором сравнил свою батарею с настоящим D-элементом на 1,5 В. Обе батареи тестировались с небольшим двигателем постоянного тока. При этом измерялся ток и скорость вращения двигателя. И самодельная и промышленная батареи показали примерно одинаковые результаты.
Конечно, этот аккумулятор не идеален. Ионообменная мембрана по-прежнему пропускает некоторые растворимые соли меди на катодную сторону батареи, где они вступают в реакцию с образованием металлической меди и нерастворимых оксидов и гидроксидов меди. Кроме того, алюминиевый катод постепенно приходит в негодность, по сути, растворяется. Но, несмотря на это, батарея очень удобна и может быть легко собрана и использована людьми в экстремальной ситуации. Увеличивая размер батареи, и подключая несколько ячеек последовательно или параллельно, можно производить или хранить очень большое количество энергии с небольшими затратами.
Источник
Магниевый аккумулятор своими руками
Добра вам!
Дорогие мои читатели, простите, что давно не писал, был поглощен работой, очень интересный проект о нем расскажу в следующей статье.
Представленная статья не принадлежит мне, взята она с блога моего товарища Крымский Лис. Оригинал ее можно прочесть тут. Я не беру обычно копипасты, но тут случай особый, затронула меня разработка, и я загорелся, деталюхами уже обзавелся останется найти время и собрать так как я хочу.
Подобные источники тока незаменимы в различных автономках – они конструктивно очень просты, в них нечему ломаться, они бесшумны, а «топливо» — легкое и безопасное. Фактически нужны только анодные пластины и соль – воду можно взять хоть из лужи. А в случае использования морской воды не требуется даже соль – хватит той, что уже растворена в воде. Источник тока работает, пока аноды полностью не растворятся. После чего нужно просто установить новые аноды, вылить отработанный электролит и залить соленую воду снова. Причем, выливать электролит можно прямо в реку или озеро – при использовании алюминиевых или магниевых анодов он экологически безвреден! Нечто подобное люди даже… употребляют внутрь – аналогичный состав у альмагеля, известного желудочного лекарства!
Комплект для батареи.
Стержень из магния минусовый
Длина 45мм
Диаметр 20мм.
Медная гильза
Длина 60мм.
Диаметр 25мм.
Элемент в разобранном виде.
Крепление минусового вывода
Ткань в качестве сепаратора
Сборка элемента
Элемент в сборе.
Электролит обычная, солёная вода.
Напряжение одного элемента 1,25 Вольта.
Моча в качестве электролита
Источник
МАГНИЙ вместо ЛИТИЯ и ЦИНКА (Новые научные решения для электрических батарей)
Технологии изготовления аккумуляторов и электрических батарей не стоят на месте. На смену традиционным Цинку и Литию и ядовитым соединениям в батареях, приходят более дешевые и безопасные материалы.
В новых аккумуляторах из Японии применяется положительный электрод, сделанный из специального полианионного соединения, удельная энергетическая емкость которого вдвое выше аналогичного параметра положительного электрода в литиевых батареях.
Электролитом в данном случае является смесь материалов Mg(TFSI)2 и Triglyme (диметиловый эфир триэтиленгликоля). При изготовлении отрицательного электрода используется магний.
На текущий момент произведено несколько прототипов аккумуляторов нового типа, которые уже находятся в стадии тестирования. По словам разработчиков, в новых АКБ отсутствует нестабильный реактив Гриньяра, что существенно повышает их надежность.
В современных литий-ионных аккумуляторах жидкий электролит переносит заряд между катодом и анодом, электрический контакт между которыми приводит к самовозгоранию аккумуляторов. Ученые из Национальной лаборатории имени Лоуренса в Беркли решили разработать более безопасную и энергоемкую магниевую батарею. Однако им оказалось сложно найти работоспособный жидкий электролит, который подошел бы магниевым батареям и не вызывал коррозию ее элементов.
Тогда решили обойти эту проблему, сделав твердотельный электролит позволяющий повысить энергоемкость и безопасность магниевых батарей.
Как отметили изобретатели, плотность магниевых аккумуляторов существенно выше в сравнении с литий-ионными , которые сейчас устанавливаются чуть ли не в каждое мобильное устройство.
Эта особенность позволит им в скором будущем получить широкое распространение. К основным компонентам нового типа АКБ относятся вышеупомянутый магний, а вместе с ним железо и кремний. Эти материалы находятся в широком доступе, что позволит снизить себестоимость элементов питания и их рекомендованную цену.
Материал, который ученые использовали — селенид магния-скандия — обладает подвижностью магния, сопоставимой с твердотельными электролитами в литиевых батареях.
В ходе экспериментов специалисты выяснили, что ионы магния могут очень быстро двигаться сквозь материал.
Источник